

原创 维生素C 医学界消化肝病频道
全是干货!
受疫情影响,2020年中国消化内镜学年会于9月11-13日在线召开。在这场会议上,来自南方医科大学南方医院的李爱民教授结合病例,详细分析了结直肠息肉早期癌变的临床处置问题。
早期结直肠癌是指癌组织局限在黏膜及黏膜下层,无论有无淋巴结转移。早期结直肠癌内镜下切除的适应证主要有黏膜内癌或黏膜下层浅层浸润癌,大小不受影响,任何肉眼类型,可以进行内镜下的完整切除。结直肠癌的早诊早治,能够显著提高患者的5年生存率,改善患者生命质量。
关键问题一
对病变性质及浸润深度作出准确的评估
会议开始,李爱民教授提出了这么一个病例:
患者女性,53岁,因“间歇性便血3月余,发现结肠息肉2周”入院,胃肠癌三项未见明显异常。
肠镜:乙状结肠距肛门20cm见1枚半球形息肉,大小约12mm×10mm,周边见白斑,表面充血,触之易出血,靛胭脂染色后观察,病变pit Vi型,用啄木鸟刀行ESD术完整剥离(2019年5月14日)。
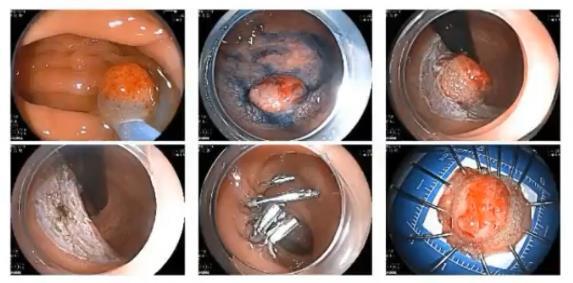
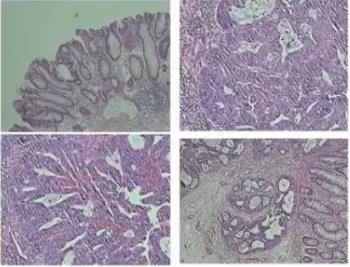
手术前(2019年5月25日)进行全腹部增强CT的评估:1.乙状结肠肠腔内多发异常密度影,考虑术后改变;2.肝S8占位性病变(2个),考虑为肝脏转移性瘤可能性大。
上腹部磁共振:肝右叶S8占位性病变,考虑为肝转移瘤。
结合上述辅助检查结果,考虑结肠癌肝转移,2019年5月31日,行腹腔镜辅助乙状结肠癌根治+肝脏肿瘤切除术+腹腔热灌注置管术。
术后病理:1.乙状结肠腺瘤切除术后未见癌细胞,双侧切缘未见病变残留;2.( Ln1、Ln2、Ln3)淋巴结均未见瘤转移;3.肝脏见癌转移,肝切缘未见癌残留。
2020年5月,外院肠镜示吻合口炎性病变,未见复发。
总体来看,这个患者的结直肠息肉处置过程中,术前的评估不够充分,走了一些弯路。
在进一步分析了南方医院近10年结肠息肉切除术后,李爱民教授指出,有12%的(26例)内镜切除术后追加了外科手术,追加外科手术后的术后病理显示肿瘤有残留的有6例(23%),淋巴结转移1例(3.85%),肝脏转移1例(3.85%)。
减少二次手术给患者带来的创伤,结直肠息肉内镜下切除前,尤其是高危腺瘤,如何进行规范化和精准的术前评估?是每一个消化内科医生应该充分重视的问题。
在内镜下结肠息肉切除术前,应该对病变性质及浸润深度作出准确的评估,是一个关键的问题。目前的主要评估方法主要有色素内镜,电子染色内镜,放大内镜,超声内镜,影像学检查等。
李爱民教授指出,我们首先还是建议采用经典的JNET分型,进行一个浸润深度的评估和病变性质的评估。
JNET分型主要看表面血管和表面结构:
1型主要对应增生性息肉,或无蒂锯齿状腺瘤。
2A型对应的病理类型一般为低级别上皮内瘤变。
2B型一般是高级别上皮内瘤变或者是黏膜下层的浅层浸润癌。
3型一般对应的是黏膜下层深层的浸润癌。

1型的血管往往不可见,如果可见也是与周围正常的黏膜一致。
2A型可以看到规则的棕黑色的微血管结构,2B型可以看到血管增粗扩张,管径不均一,不规则分布的血管结构。
3型可以看到无血管区。
JNET表面形态:
1型可以看到黑白点状均一可见的表面结构。
2A型可以看到管状分支状规则的表面结构,对应pit分型的Ⅲ型或者Ⅳ型。
2B型可以看到不规则的表面结构,对应pit分型的Vi型(2B又分为2B低级和2B高级,2B低级指不规则增粗的血管分布比较均匀,2B高级指不规则增粗的血管分布不均匀)。
3型,表面结构消失,对应pit分型的ⅤA型。
基于JNET分型的结直肠早癌处理策略:
1型可以继续随访。
2A及2B低级需要内镜下切除。
2B高级需要进一步结合放大色素染色内镜,以及pit分型,进一步准确的评估,来决定后续的处理策略。
3型建议直接外科手术。
pit分型
Ⅰ型:正常的圆形的血管开口。
Ⅱ型:星状的开口。
ⅢS型:比正常的pit小的圆形的腺管开口,ⅢL型比正常的大的腺管开口。
Ⅳ型:树枝状、脑回状的腺管开口(Ⅱ型到Ⅳ型都是规则的结构)。
ⅤA型:不规则分布的ⅢS、ⅢL、 Ⅳ型,混杂分布。
ⅤN型:开口减少或消失。
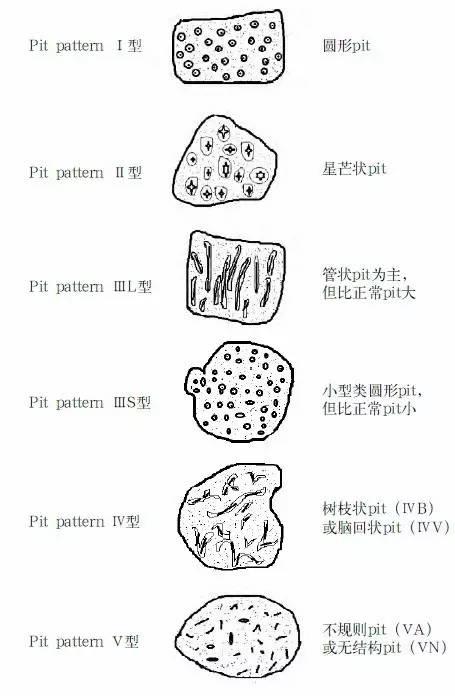
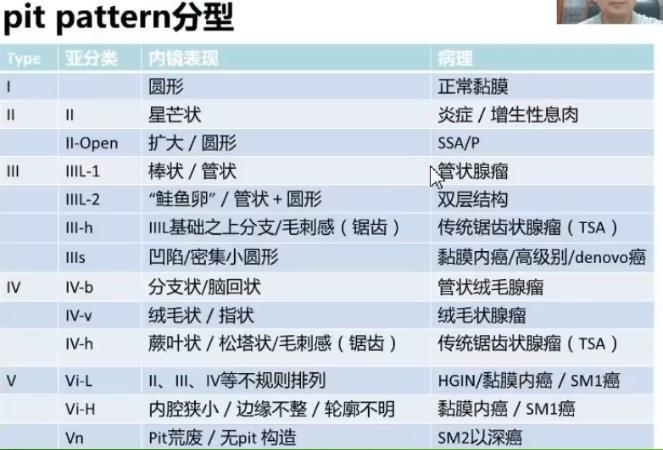
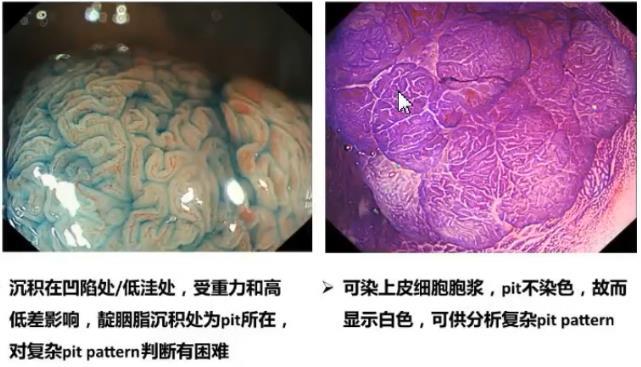
色素染色放大观察腺管开口的形态,靛胭脂沉积在凹陷处、低洼处,受重力和高低差影响,靛胭脂沉积处为pit所在,对复杂pit判断有困难。结晶紫可染上皮细胞胞浆,pit不染色,故而显示白色,可供分析复杂pit。
����滑动查看
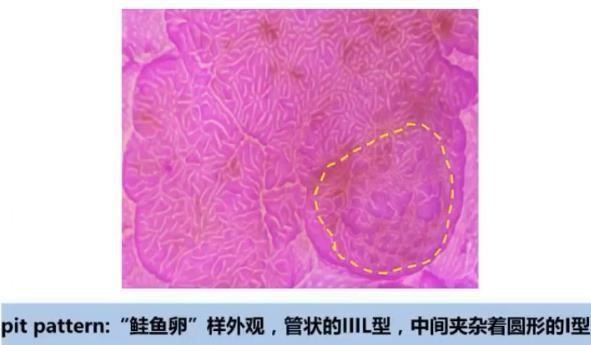
第1步观察微血管和表面的结构,发现病变介于2A和2B之间,用色素内镜进一步评价微表面的结构,经染色后观察pit分型为鲑鱼卵样外观,管状的ⅢL型,中间夹杂着圆形的Ⅰ型,因此这个病变是ⅢL和Ⅰ型混杂,也就是ⅢL-2型。
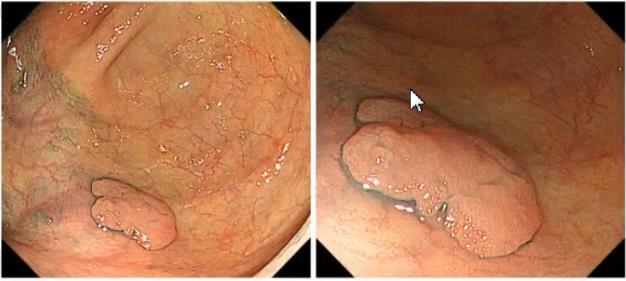
下面,李爱民教授以一个病例为例,分析了超声内镜在术前评估中的应用价值:
����滑动查看
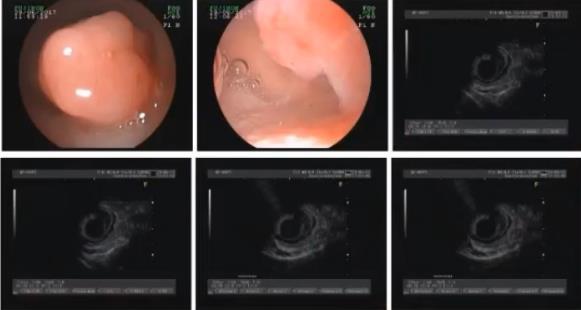
53岁男性,主诉为便血3月,于加重11天;肠镜见直肠巨大肿物。
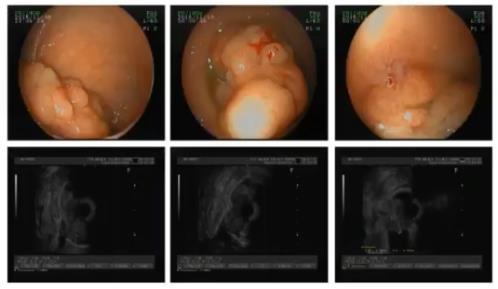
关键问题二
合理内镜治疗方法的选择
完成结直肠息肉术前评估后,另一个需要注意的问题就是合理内镜治疗方法的选择。
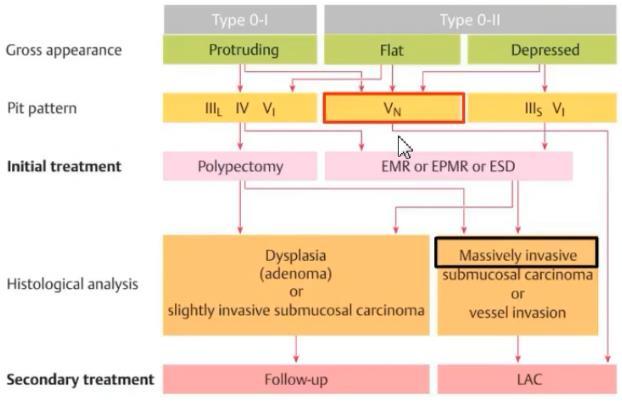
关于这个问题,2015年的专家共识给出了明确的建议,带蒂或者是亚蒂的隆起性病变,直接行圈套器切除。对于扁平隆起型腺瘤、LST、局限于黏膜内、黏膜下浅层的早癌,直径小于20mm者,直接EMR切除;直径大于20mm者内,镜下能切除者可以性EPMR或ESD,内镜不能切除的,建议外科手术。经过评估,如果是黏膜下层深层浸润癌,建议外科手术。
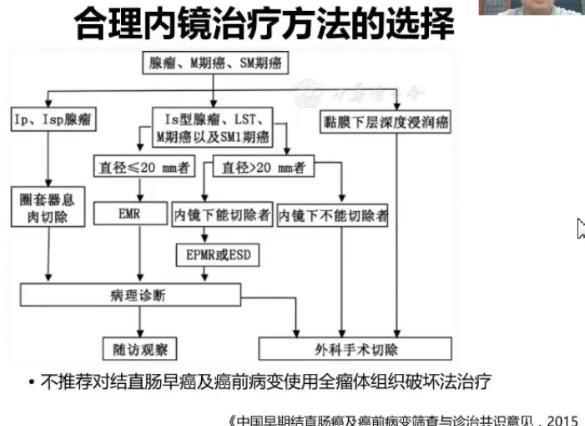
精准病理诊断的评估
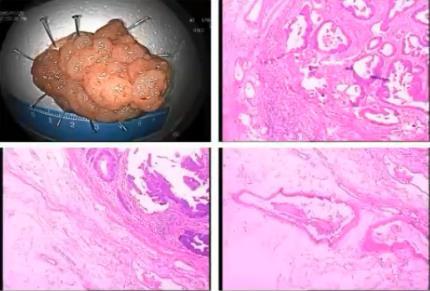
内镜下手术切除结直肠息肉后,手术标本的规范化的病理评估,对于指导患者后续的治疗是至关重要的。
手术标本的规范化的病理评估,对于指导患者后续的治疗是至关重要的,主要包括两个方面,第一方面是规范化的标本处理流程,包括黏膜标本需要充分的平展,做好标本方位的标识,如肛侧、口侧。从垂直于肿瘤最近距离的黏膜切缘,进行切取,每间隔2-3mm平行切开保护息肉蒂部的完整性,充分展示基底切缘。
另一个方面就是规范化的病理报告的书写。

接下来李爱民教授分享了一个病例:
����滑动查看
2017年6月27日,肠镜检查:距肛缘16cm见一宽基息肉,直径约20mm,色红,表面有分叶,CPⅡ型,pitVi(高度不整),充分吸气及注气,病变基底柔软,黏膜下注射病变抬举征良好。
结论:乙状结肠宽基病变,考虑为早期肿瘤。
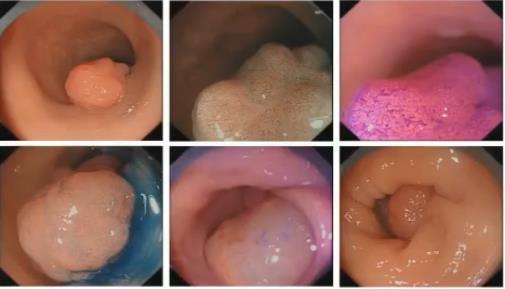
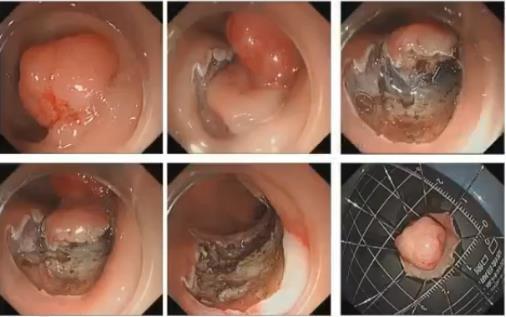
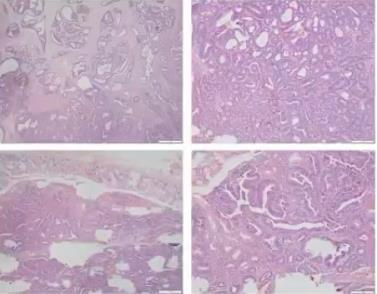
2017年11月于全麻下行腹腔镜辅助直肠切除术,诊断直肠中分化腺癌(pT4aN2aM0)。
这个病例给我们一个教训,虽然术前进行了术前浸润深度和性质的评估,术后也进行了病理评估,但忽略了免疫组化脉管浸润的分析和判断,导致了术前评估的不充分,最终导致ESD后结肠癌复发和周围淋巴结转移。
关键问题四
后续治疗策略的选择
根据病理评估的结果,制定患者后续治疗及随访方案。

密切随访
最后就是随访的问题,我们需要根据患者不同的情况制定不同的随访策略,根据日本的指南的建议,整块切除并且切缘阴性,推荐术后一年左右行内镜检查。pTis癌分片切除且水平切缘阳性,推荐6个月左右行内镜检查。pT1癌未追加肠切除,除内镜检查外,还需CT和肿瘤标志物监测淋巴结复发和远处转移。
小结一下
结直肠息肉早期癌变的临床处置需要注意的5大关键问题:
第一,术前浸润深度的评估。
第二,内镜手术方式的选择。
第三,术后病理规范化评估。
第四,决定是否追加外科手术。
第五,密切随访。
专家简介
李爱民教授
南方医科大学南方医院消化科副主任
南方医院增城分院消化科主任
广东省胃肠疾病重点实验室副主任,硕士生导师
主持中国博士后科学基金1项、国家自然科学基金1项、省级科研项目3项,第一及通讯作者发表SCI论文10篇、获国家专利授权9项、担任副主编出版专著1部,2017年获广东省科技进步一等奖
本文首发:医学界消化肝病频道
汇报专家:李爱民
本文作者:维生素C